Відоме міжнародне видання опублікувало статтю про сквален, одним із авторів якої є вчений інституту фізики НАН України
Ми вже неодноразово писали, що один з основних елементів амаранту і амарантової олії — сквален. Він неймовірно корисний для організму, як при зовнішньому, так і внутрішньому застосуванні. Його все активніше використовують при виробництві косметичних препаратів і лікарських засобів. При цьому — тривають дослідження сквалену, що відкривають нові можливості речовини. І демонструють, наскільки важливим є вирощування амаранту. Сьогодні ми хочемо представити вашій увазі чергові результати досліджень — про них повідомляє Національна Академія Наук України (http://www.nas.gov.ua).
Публікація в журналі Nature Communications
30 травня 2017 в престижному журналі «Nature Communications» вийшла стаття «Кон’югація сквалену з гемцитабином як унікальний підхід до доставки ліків, використовуючи ендогенні ліпопротеїни».
Одним з її співавторів в складі великого міжнародного авторського колективу є провідний науковий співробітник відділу фізики біологічних систем Інституту фізики НАН України, доктор фізико-математичних наук Семен Есилевський.
Робота виконана в області наномедицини — найважливішого міждисциплінарного наукового напрямку на перетині медицини, молекулярної біології, біофізики, біохімії і фармакології, що займається застосуванням наночастинок з лікувальною та діагностичною метою.
Основною проблемою сучасної фармакології (особливо при лікуванні онкологічних захворювань) є точна, адресна доставка токсичних лікарських речовин до пухлини і мінімізація її впливу на здорові тканини і організм в цілому.
Наномедицина пропонує «упаковувати» ліки в інертні наночастинки-контейнери, переносити їх до клітин-мішеней і звільняти тільки там, де це необхідно.
Зазначене завдання вкрай складне, адже потрібно розробити способи отримання наночастинок, упакувати в них ліки для адресної доставки в обрані клітини, забезпечити контроль вивільнення, утилізації наночастинок організмом тощо.
Зараз повністю вирішити цю задачу поки ще не вдалося, проте вчені поступово наближаються до використання наночастинок в медичній практиці.
З історії наномедицини
За майже 30 років існування наномедицини було запропоновано величезну кількість варіантів терапевтичних наночастинок. Їх виготовляли на основі:
- різних полімерів;
- ліпосом (ліпідних бульбашок);
- металевих наночастинок (заліза, золота, срібла, міді);
- карбонових матеріалів (фулеренів, нанотрубок, графену);
- і безлічі інших матеріалів і їх комбінацій.
На жаль, жоден з цих варіантів не дійшов до широкої медичної практики. Згодом стало зрозуміло, що для досягнення бажаного ефекту найкраще підходять наночастинки з нетоксичних біосумісних матеріалів, які можуть розпадатися і утилізуватися в організмі, не завдаючи шкоди здоровим органам і тканинам.
Сквален, як біологічно сумісний матеріал
Одним з найбільш перспективних біосумісних матеріалів нині є сквален — жиророзчинна речовина постійно синтезується в клітинах нашого організму як попередник в синтезі холестерину і стероїдних гормонів.
Сквален — нейтральна і абсолютно нешкідлива речовина, яка вже давно широко використовується в парфумерії та косметології. Фахівці групи професора Патріка Кувре (Patrick Couvreur) з Університету Парі-Зюд (м. Париж, Франція) є піонерами у використанні сквалену для створення терапевтичних наночасток. Вони, зокрема, розробили технологію хімічної модифікації ряду лікарських препаратів скваленовими «хвостами», після якої такі агрегати починають формувати наночастинки різної форми і розміру.
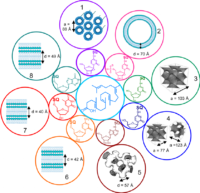
Сквален (в центрі), його похідні і структури, які вони формують у складі наночастинок.
Вже досить давно відомо, що скваленові наночастинки нетоксичні і можуть бути введені безпосередньо в кров, яка успішно транспортує їх до відповідних тканин-мішеней. У той же час, вчені не знали, як такі частинки взаємодіють з різними компонентами плазми крові.
Власне, з’ясування цих механізмів і стало метою дослідження, в якому взяв участь С. Есилевський. Роботи проводилися за допомогою комбінації експериментальних методик і комп’ютерного моделювання. В останні роки це — своєрідний «золотий стандарт» для біомедичних досліджень.
Взаємодія сквалену з ліпопротеїнами плазми крові: вивчення ефективного методу боротьби проти раку
Оскільки сквален є жиророзчинною речовиною, то особливу увагу вчені приділили вивченню його взаємодії з ліпопротеїнами плазми крові.
Ліпопротеїни — це складні природні наночастинки, синтезовані людським організмом для перенесення кров’ю речовин, нерозчинних у воді, зокрема ліпідів і холестерину.
Особливу роль в цьому процесі відіграє фракція ліпопротеїнів низької щільності, яку в побуті часто називають «поганим холестеролом», адже його надлишок часто спостерігається у осіб, хворих на атеросклероз. Дуже спрощено ліпопротеїни можна описати як нанорозмірні жирові краплі, покриті поверхневим шаром ліпідів і білків.
Під час дослідницької роботи виявилося, що скваленові наночастинки дуже активно взаємодіють з ліпопротеїнами низької щільності в плазмі крові.
Комплекс протиракового препарату гемцитабіну з скваленом (гемцитабін-сквален) вбудовується в ліпопротеїнові частки і разом з ними поширюється по організму. Скваленовий «хвіст» при цьому виконує функцію якоря: завдяки своїй жиророзчинності він проникає всередину ліпопротеїнової жирової краплі, втягуючи за собою приєднану молекулу гемцитабіну. Без скваленового «хвоста» цей водорозчинний препарат не проникає в ліпопротеїнові частки і швидко деградує в плазмі крові, не досягаючи клітин-мішеней.
Вбудовування гемцитабін-сквалену в ліпопротеїни дуже важливе ще і з огляду на те, що ракові клітини часто мають підвищену потребу в холестеролі і захоплюють з крові значно більшу кількість ліпопротеїнів, ніж здорові клітини. Таким чином, лікарський препарат у високих концентраціях адресно доставляється до ракових клітин-мішеней.
Група професора Патріка Кувре виконувала основну експериментальну частину роботи, а український вчений Семен Есилевський разом з професором Крістофом Рамзеером з Університету Бурґонь-Франш-Комте (м. Безансон, Франція) проводили комп’ютерне моделювання процесу вбудовування гемцитабін-сквалену в ліпопротеїни низької щільності за допомогою методу молекулярної динаміки.
Розглядалася модельна система з декількох сотень тисяч атомів, яка складалася з молекули гемцитабін-сквалену і частини ліпідного ядра ліпопротеїнової частки. Всі фізичні міжатомні взаємодії та рух всіх атомів в такій системі розраховували явно.
Було доведено, що для молекули гемцитабін-сквалену проникнення в ліпопротеїнову частинку є енергетично вигідним, тоді як сам гемцитабін всередину не проникає. Отже, розрахунки повністю підтвердили експериментальні дані.

Молекула гемцитабін-сквалену всередині ліпопротеїнової частки (миттєвий знімок системи при моделюванні методом молекулярної динаміки)
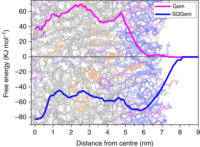
Профілі вільної енергії перенесення гемцитабіну (рожевий) і гемцитабін-сквалену (синій) з води всередину ліпопротеїнової частки (негативні значення енергії відповідають спонтанному зв’язуванню)
Підводячи підсумок
В цілому, ця робота пояснює тільки одну з численних деталей великої і дуже складної картини поведінки скваленових наночастинок в живому організмі.
Однак саме такі дрібні деталі поступово наближають науку до створення нових ефективних лікарських препаратів.















Виникла якась проблема :(